Por Dra. María de los Ángeles Nannini.
Presidente del Comité de Chagas 2021.
INTELIGENCIA ARTIFICIAL Y ECOCARDIOGRAFÍA: GUÍA PARA ECOCARDIOGRAFISTAS
Artificial Intelligence and Echocardiography: A Primer for Cardiac Sonographers.
Davis A, Billick K, Horton K, et al. J Am Soc Echocardiogr 2020;33:1061-6.
Por Dra. Silvana López.
Presidente del Comité de Imágenes no invasivas y ecografía 2020.
ESTILO DE VIDA E IMPACTO EN EL CONTROL DE FACTORES DE RIESGO CARDIOVASCULAR EN PACIENTES CORONARIOS EN 27 PAÍSES: RESULTADOS DEL REGISTRO EUROASPIRE V DE LA SOCIEDAD EUROPEA DE CARDIOLOGÍA.
Por Dr. Nicolás Chichizola.
Presidente del Comité de Cardiología del Ejercicio 2020.
Dra. Carolina Chacón.
Autora: Dra. Cristina B. Sorribas
1- ¿Hay estadísticas en nuestro país sobre incidencia y morbimortalidad relacionadas con hipertensión y embarazo?
ARTÍCULOS COMENTADOS POR COMITÉS
ARTÍCULOS COMENTADOS POR COMITÉS
Comité de Cardiopatías Congénitas 2020
Autor: Juan Pablo Argüello.
Pregnancy in Women with Complex Congenital Heart Disease. A Constant Challenge
Avila WS, Ribeiro VM, Rossi EG, et al. Arq Bras Cardiol. 2019; 113(6):1062-1069
La mejora en las técnicas quirúrgicas ha contribuido a un número creciente de mujeres en edad fértil con cardiopatía congénita compleja (CCC). Sin embargo, el asesoramiento adecuado sobre el embarazo en esta situación es incierto, debido a una amplia variedad de lesiones cardíacas residuales.
ARTÍCULOS COMENTADOS POR COMITÉS
Comité de Arritmias y Electrofisiología
Dr. Sebastián Nannini
LA TAN ESPERADA PUBLICACIÓN DEL ESTUDIO CABANA.
Efecto de la Ablación por Catéter vs Tratamiento con Drogas Antiarrítmicas en mortalidad, stroke, sangrado y paro cardíaco entre pacientes con Fibrilación Auricular.
Effect of Catheter Ablation vs Antiarrhythmic Drug Therapy on Mortality, Stroke, Bleeding, and Cardiac Arrest Among Patients With Atrial Fibrillation: The CABANA Randomized Clinical Trial.
Packer DL, Mark DB, Robb RA, et al.
JAMA. 2019;321(13):1261-1274.
Después de mucho tiempo llegó el momento de la publicación del estudio CABANA, esperado tanto por cardiólogos como por electrofisiólogos. Este se trata de un estudio multicéntrico (126 centros en 10 países), abierto, randomizado, cuyo objetivo fue determinar si la ablación por catéter de la Fibrilación Auricular (FA) es más efectiva que el tratamiento farmacológico habitual para disminuir eventos cardiovasculares y mortalidad.
Se randomizaron 2204 pacientes (p) con FA sintomáticos desde el 11/2009 al 04/2016. Los criterios de inclusión fueron: p mayores de 65 años o menores con 1 o más factores de riesgo para ACV y que sean candidatos para ablación o tratamiento médico que controle ritmo o frecuencia. Se excluyeron aquellos p con ablación previa o refractarios a 2 o más fármacos antiarrítmicos.
La ablación consistió en el aislamiento de las venas pulmonares quedando otras técnicas a discreción de cada centro. Los médicos operadores debían tener más de 100 procedimientos de experiencia. Todos los p debían recibir anticoagulación según las guías.
El punto final primario fue un combinado de muerte, ACV discapacitante, sangrado serio y paro cardíaco y de los 13 puntos finales secundarios sólo se informaron en este artículo mortalidad por todas las causas, mortalidad total u hospitalización cardiovascular (CV) y recurrencia de FA.
El seguimiento se realizó a los 3, 6 y 12 meses y luego cada 6 meses. Los eventos fueron revisados y adjudicados en forma ciega por un comité independiente. Para registrar la recurrencia se les dio a los p una grabadora de eventos activada por síntomas o automáticamente durante el día y con un holter de 96 hs cada 6 meses. Cualquier episodio de FA de más de 30 segundos se consideró recurrencia. Se definió un período de blanking de 3 meses en ambos grupos donde no se buscaron recurrencias.
Resultados:
Un total de 2204 p fueron randomizados a ablación (1108 p) o fármacos (1096 p). El seguimiento medio fue de 48,5 meses. La edad promedio de los p fue de 68 años, 37% fueron mujeres y 10% pertenecían a minorías raciales y étnicas.
La FA paroxística estuvo presente el 42% de los p, y el 80% de los p tenían algún factor de riesgo cardiovascular.
De los p asignados a ablación el 90% se la realizó. El 19% de estos fue sometido a otro procedimiento. El 44% de los pertenecientes a este grupo recibió fármacos antiarrítmicos pero sólo el 26% al final del seguimiento.
El 99% de los p asignados a fármacos los recibieron, Hubo un 27% de cruzamiento al grupo intervención.
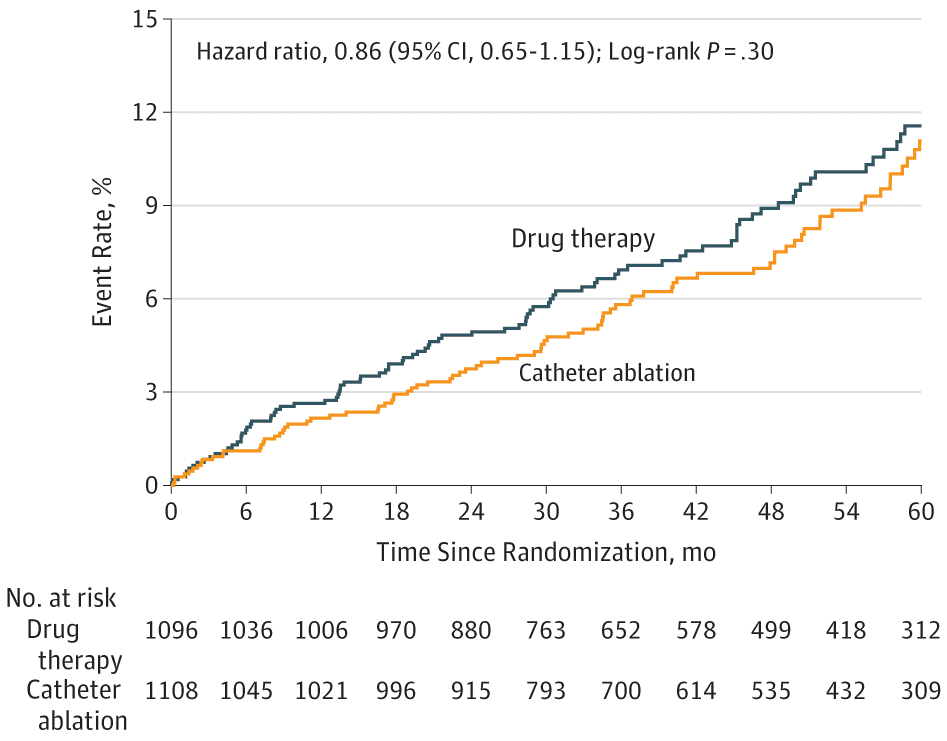
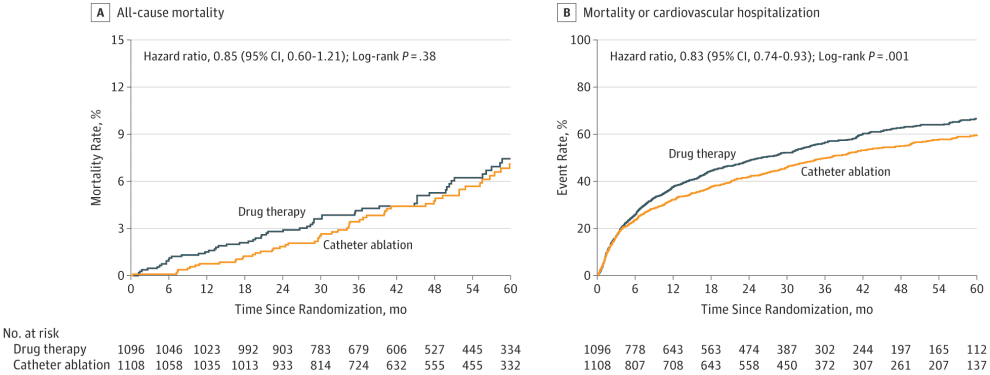
Según el análisis por intención de tratar, el punto final primario no tuvo diferencias en ambos grupos el hazard ratio (HR) fue 0,86 (p=0,3). (Fig. 1) Tampoco la hubo para los puntos finales secundarios excepto para el combinado de Mortalidad y Hospitalización Cardiovascular HR 0,83 (p=0,001). (Fig. 2).
Sin embargo según el análisis por tratamiento recibido el HR del punto final 1° fue de 0,67, para mortalidad por todas las causas fue de 0,60 y para el combinado de muerte y hospitalización CV fue de 0,83, todos con p significativas.
En 1240 p con grabador de eventos la disminución de recurrencia post blanking fue del 48% (p=0,001) a favor de la ablación.
Los efectos adversos fueron infrecuentes, en el grupo ablación hubo un 0,8% de taponamiento cardíaco y en el grupo farmacológico los desórdenes tiroideos fueron reportados en el 1,6% mientras que la proarritmia en el 0,8%.
Discusión:
Luego de 8 años de espera se publicaron los datos del estudio CABANA. Es el primer estudio randomizado que comparó la ablación por catéter y el tratamiento médico para puntos finales duros como muerte, ACV discapacitante, sangrado serio y paro cardíaco en pacientes con FA.
Cabe aclarar que el punto final primario original era mortalidad pero fue cambiado por el combinado por una enmienda en el 2013 debido al lento enrolamiento y a la baja tasa de eventos en el grupo farmacológico.
Si bien se calculó un cruzamiento del 25%, la falta de cumplimento de la ablación en el 9,2% podría haber afectado los resultados del estudio.
El análisis por intención de tratar es la única forma que garantiza la comparación de los grupos y los eventos sufridos por ellos. Por lo tanto, esta apreciación convierte al CABANA en un estudio negativo.
Sin embargo el estudio no deja de ser importante, ya que avala la actual indicación de la Ablación de FA en pacientes sintomáticos debido a la menor recurrencia en comparación con el tratamiento médico sin una alta tasa de complicaciones graves.
Figura 1
Figura 2
Traducido de Packer DL, et al. Effect of Catheter Ablation vs Antiarrhythmic Drug Therapy on Mortality, Stroke, Bleeding, and Cardiac Arrest Among Patients With Atrial Fibrillation: The CABANA Randomized Clinical Trial. JAMA. 2019;321(13):1261-1274.